폐 실질 이상(lung parenchymal abnormality)은 폐의 실질(parenchyme)이 섬유화나 파괴를 비롯한 다양한 형태로 이상한 구조를 영상에서 보이는 상태를 의미합니다. 이 중 가장 대표적인 질환군은 간질성 폐 질환(interstitial lung disease; ILD)이라고 할 수 있고요. 의과대학에서 배우는 ILD의 생리학적인 소견은 폐기능검사상 FEV1/FVC가 유지되지만 FVC와 FEV1 자체의 값은 낮아져 있는 restictive pattern을 띈다는 것입니다.
하지만 진단과 치료에서 예방으로 넘어가는 21세기의 의학 관점에서 시판중인 치료제가 두 가지밖에 없고(pirfenidone, nintedanib - nerandomilast는 현재 임상 및 승인 진행중) ILD는 비가역적으로 폐가 섬유화되기 때문에 다시 정상으로 돌아갈 수 있는 방법은 2024년 현재에는 없으므로 어찌 보면 예방이 더 중요한 것 같습니다. 따라서 ILD를 조기에 진단하고 예방하는 것이 ILD를 치료하는데 있어서 만큼이나 중요한 것으로 간주될 수 있습니다.
일반적으로, 영상의 조그마한 변화는 폐기능검사(spirometry, pulmonary function test; PFT)상에서는 감지가 힘들기 때문에 ILD의 초기 단계는 PFT보다 영상에서, 특히 CT 영상에서 더 민감하게 잡히는 것으로 알려져있곤 합니다. 이렇게 폐기능검사는 이상이 없지만 영상에서는 비정상 폐실질 소견을 보이는 것을 subclinical parenchymal lung disease라고 부르기로 합시다[Ref 1].
Subclinical parenchymal lung disease를 처음으로 접근한 2009년의 연구[Ref 1]는 airflow obstruction이나 clinical cardiovascular disease가 없는 2,563명의 흡연자들을 대상으로 한 Multi-Ethnic Study of Atherosclerosis (MESA) study라는 cohort에서 수행되었습니다. NHANES I cohort를 사용한 이전 연구[Ref 2]에서는 현재 흡연 여부가 spirometric restriction과 관련이 있다는 것을 보였지만 폐암에서와 같이 갑년(pack-years)에 대한 분석은 없었기에 해당 연구는 subclinical parenchymal disease를 -600HU에서 -250HU 사이의 high attenuation area (HAA)로 정의하고 분석을 수행하였습니다. 이 HU 범위는 ground-glass opacity (GGO)와 reticulation을 포함하고 vessel이나 complete atelectasis, nodule을 제외할 만큼 낮은 적당한 범위였습니다. 결론적으로 흡연과 HAA는 상관관계가 발견되었고 spirometric restriction과 HAA도 상관관계가 발견되었습니다. 이 때 까지는 ILA에 대한 학문적 정의도 없던 시절이었다는 것을 기억하면 해당 연구는 선구적인 관점을 제시했다고 할 수 있습니다.
2010년에 수행된 일본 그룹의 연구[Ref 3]에서는 폐암 검진을 위해 촬영한 환자들에게서 Klebs von der Lungen-6 (KL-6), surfactant protein (SP)-A, SP-D, PFT, 그리고 CT간의 상관관계를 연구하였습니다.
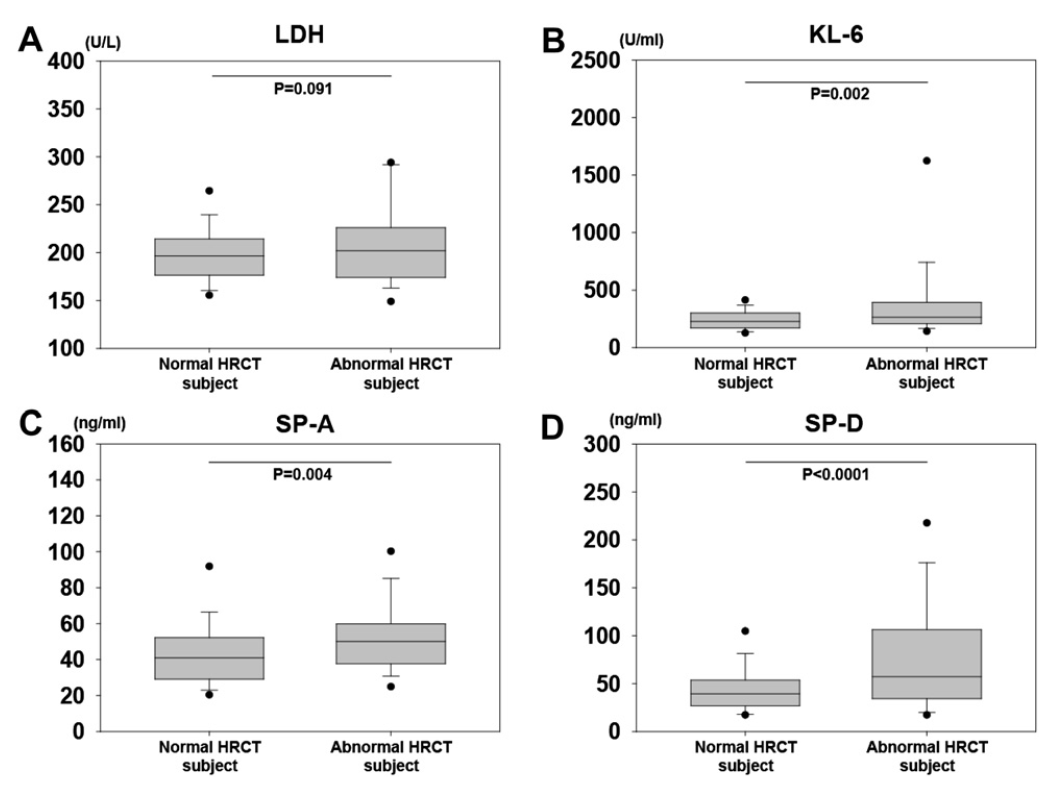
정상 군과 high resolution CT (HRCT) 사이에서 biological marker들이 어느 정도 차이를 보이는 것을 확인할 수 있었고 4년간의 추적관찰을 수행한 결과 usual interstitial pneumonia (UIP) 패턴을 보이는 환자 4명을 역추적하여 interlobular septal thickening (IST) 패턴이 흔하게 발견되었으나 다수의 환자들에게서는 interstitial lung abnormality (ILA)가 5% 미만으로 발견되었습니다.
2010년에 발간된 다른 연구[Ref 4]는 COPDGene study에서 CT로 ILA의 검출과 평가가 유용하다는 것을 증명했고, 2011년의 NEJM 연구[Ref 5]에서는 흡연자의 1/12 정도가 ILA를 가지고 있고 이들의 total lung capacity가 떨어져있다는 것을 보였습니다. 이후에는 관련 연구들이 쏟아져 나오며 ILA에 대한 이해도는 높아져 왔습니다.
이렇게 ILA 관련 연구들이 홍수처럼 쏟아지고 있던 도중 발간된 position paper이 바로 Fleischner society의 position paper, “Interstitial lung abnormalities detected incidentally on CT: a Position Paper from the Fleischner Society” 입니다[Ref 6]. 먼저, 이 position paper은 CT에서 incidental하게 발견된 ILA만을 대상으로 합니다. 따라서 ILD가 의심되어 HRCT를 촬영한 환자들과 같은 그룹은 대상이 아니라는 것이죠. 아래 표는 ILA의 유병률과 사망에 대한 hazard ratio를 정리한 자료입니다.
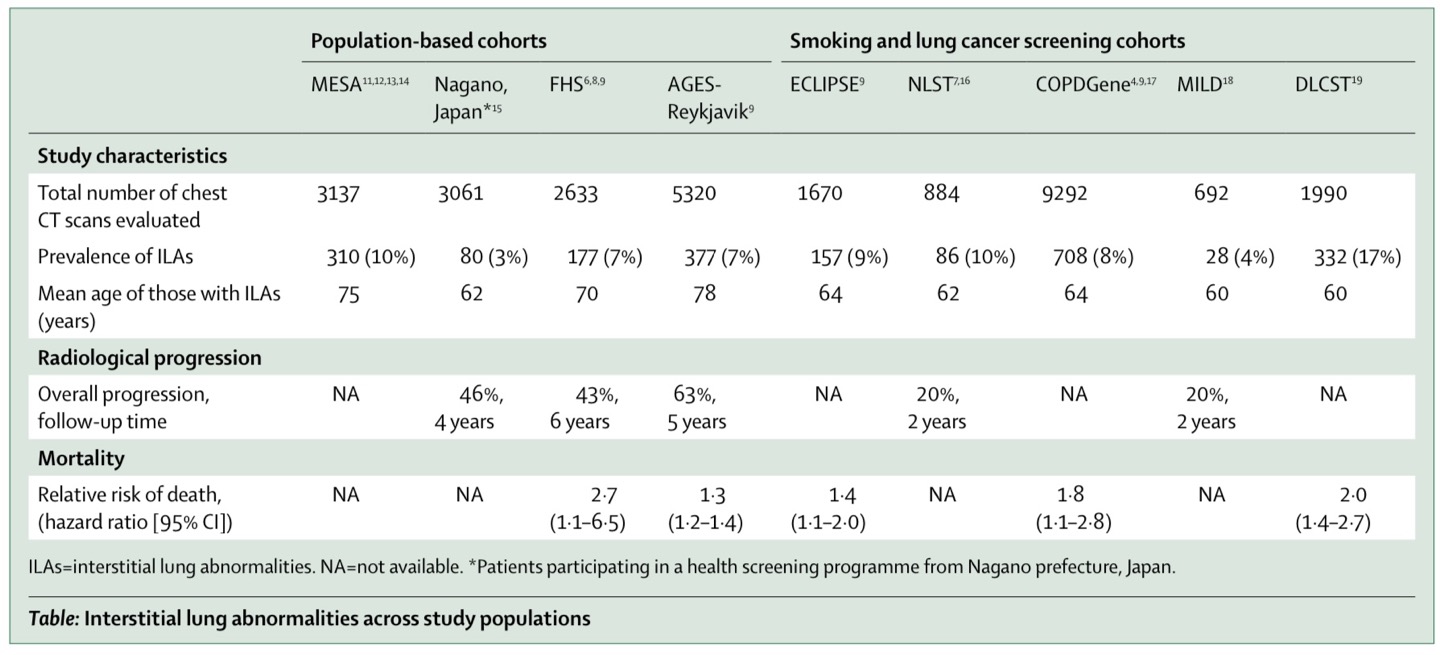
이 position paper에서는 ILA를 subclinical ILD와 동의어로 두지 말라고 하는데, subclinical ILD는 단어가 시사하듯 subclinical, 즉 임상적 증상이 나타나기 전/나타나지 않은 상태의 ILD이지만 ILA는 폐기능검사상의 이상이나 증상의 발현이 있을 수 있기 때문입니다. 이 position paper에서는 이전의 연구들을 종합하여 다음의 소견들이 prognosis에 영향을 주는 finding들이라고 하였습니다: (1) traction bronchiectasis, (2) architectural distortion, (3) honeycombing. 이들은 fibrosis의 근거이기에 ILD로 진행할 가능성이 높고 나쁜 예후와 관련이 되어 있는 것이지요.
Fleischner position paper에서는 ILA를 다음처럼 정의합니다.
- Incidental finding이면서,
- Non-dependent abnormality여야 함. (dependent atelectasis와 같은 소견들이 의심되면 prone을 찍어 rule-out 해야 함.)
- 이 abnormality에는 예를 들어 GGO, reticular abnormality, lung distortion, traction bronchiectasis, honeycombing, non-emphysematous cyst등이 포함됩니다.
- Inferior aortic arch와 right inferior pulmonary vein을 기준으로 좌우 폐를 각각 upper, middle, lower lung zone으로 (총 6개 영역. Lobe이 아닙니다.) 으로 나누어 5% 이상 침범했다는 소견을 검증해야 합니다.
그런데 5%라는 기준은 사실 인간이 정량적으로 눈으로 측정하기는 어렵습니다. 영상의학과 의사의 주관적 판단에 의거한 기준이기 때문에 Quantitative CT (QCT)가 필요하게 되고 상용화된 제품으로는 한국의 코어라인소프트의 AVIEW 제품이 이러한 정량화를 해줍니다. 아래 사진처럼, abnormal lung area를 fibrotic ILA와 non-fibrotic ILA로 분할하고 lung zone에 따라 5% 이상 침범한 영역이 어디에 있는지를 모식도로 나타내 줍니다.
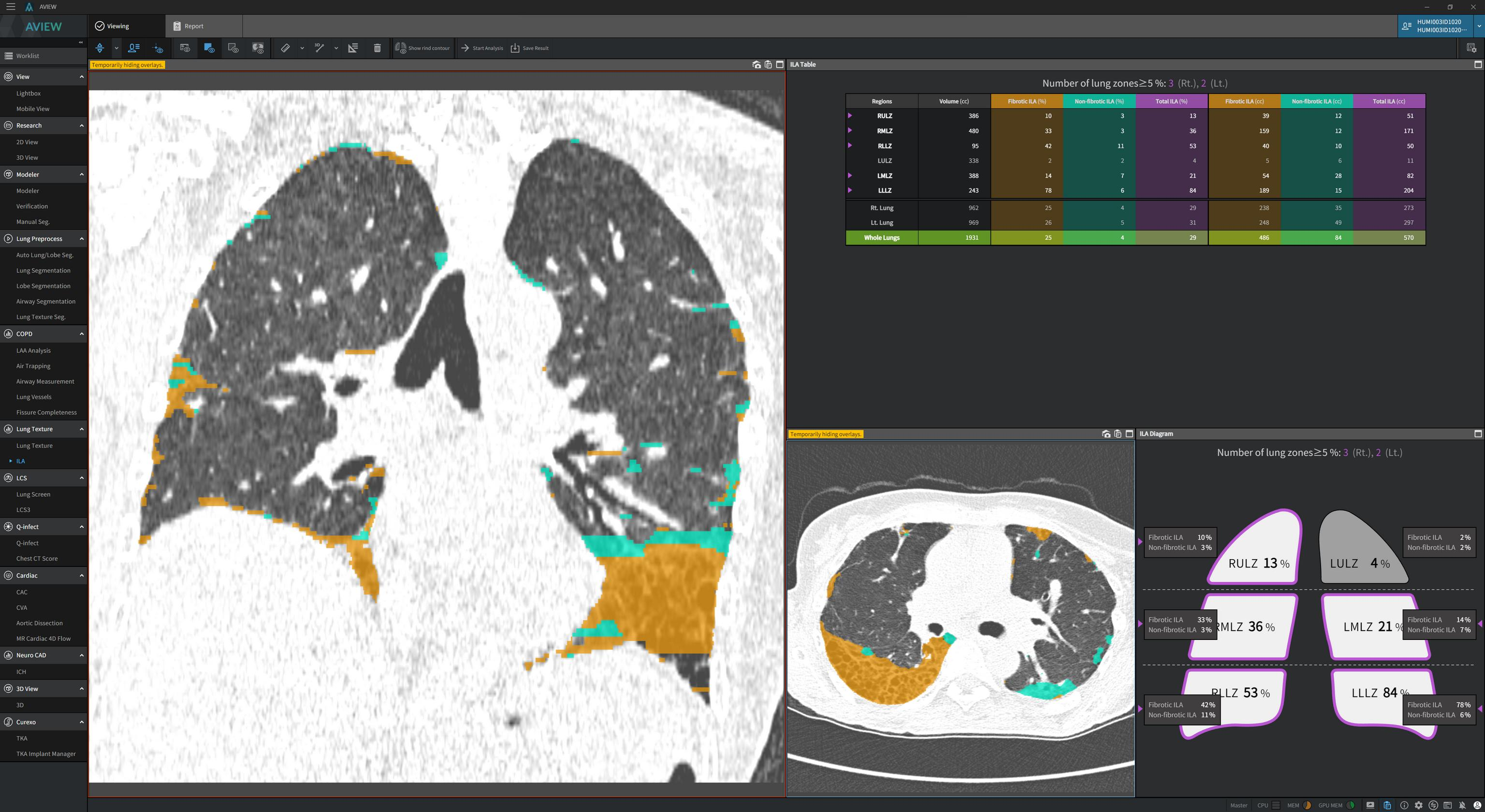
이러한 연구들을 바탕으로 Radiology에 Reviews and Commentary로 ILA의 State of the Art라는 글이 올라오기도 했고[출처 7] ILA의 조기 진단과 관리에 관한 연구들이 쏟아지고 있는 중입니다. 그럼에도 불구하고 lung fibrosis를 되돌릴 수 있는 약제는 아직 없는 것이 현실이고, ILD가 아닌 ILA에 anti-fibrotic drug를 쓰는 것이 cost와 effectiveness 둘 다에 긍정적인 효과가 있는지도 검증되지 않았습니다.
그럼에도 불구하고, ILD라는 무서운 질환을 이겨내기 위해서는 끊임없는 연구와 개발이 필요할 것입니다. Staying ahead of symptoms!
References
- Lederer, David J., et al. “Cigarette smoking is associated with subclinical parenchymal lung disease: the Multi-Ethnic Study of Atherosclerosis (MESA)–lung study.” American journal of respiratory and critical care medicine 180.5 (2009): 407-414.
- Mannino, D. M., et al. “Risk factors for prevalence of and mortality related to restriction on spirometry: findings from the First National Health and Nutrition Examination Survey and follow-up.” The International Journal of Tuberculosis and Lung Disease 9.6 (2005): 613-621.
- Tsushima, Kenji, et al. “The radiological patterns of interstitial change at an early phase: over a 4-year follow-up.” Respiratory medicine 104.11 (2010): 1712-1721.
- Washko, George R., et al. “Identification of early interstitial lung disease in smokers from the COPDGene Study.” Academic radiology 17.1 (2010): 48-53.
- Washko, George R., et al. “Lung volumes and emphysema in smokers with interstitial lung abnormalities.” New England Journal of Medicine 364.10 (2011): 897-906.
- Hatabu, Hiroto, et al. “Interstitial lung abnormalities detected incidentally on CT: a Position Paper from the Fleischner Society.” The lancet Respiratory medicine 8.7 (2020): 726-737.
- Hata, Akinori, et al. “Interstitial lung abnormalities: state of the art.” Radiology 301.1 (2021): 19-34.
