인공지능이건 아니건 어떠한 의료기기를 만들고 나면, 미국 시장이 가장 크고 매력적으로 다가오기 때문에 미국으로 눈을 돌릴 수밖에 없습니다. 이 글에서는 미국 의료기기 시장에 진입하게 되는 가장 기본적인, 그리고 포괄적인 루트들과 NEJM AI에 실린 미국 인공지능 의료기기 현황을 살펴보도록 합니다.
의료기기는 일반적인 상용 제품과 달라서 제작에 성공한다 하더라도 세 가지 주체가 분리되어 있습니다. 그것은 바로
- 의료기기를 사용하는 주체 - 의사 및 의료진
- 의료기기를 지불하는 주체 - 정부와 환자가 함께 의료기기 사용에 대한 비용 을 지불합니다.
- 의료기기의 사용을 통해 수혜받는 주체 - 환자.
라는 것입니다. 일반적인 공산품 혹은 소프트웨어는 1, 2, 3이 모두 동일한데 비해(ChatGPT를 생각해 보세요.), 의료기기는 이 주체들이 분리되어 있습니다. 따라서 시장의 구조가 복잡해지고 세 주체의 니즈를 모두 충족하는 것이 힘들게 되지요.
제가 이전 글에서도 다루었듯 의료기기의 비용 지불은 각 국가의 보험 구조와 밀접하게 연관되어 있을 수밖에 없습니다. 위 글에서 저는 수가라는 것이 의료기기 사용의 핵심 원동력이 된다고 했는데요, 미국에서 수가를 정하는 집단은 크게 세 집단 - CMS, AMA, FDA로 볼 수 있습니다.
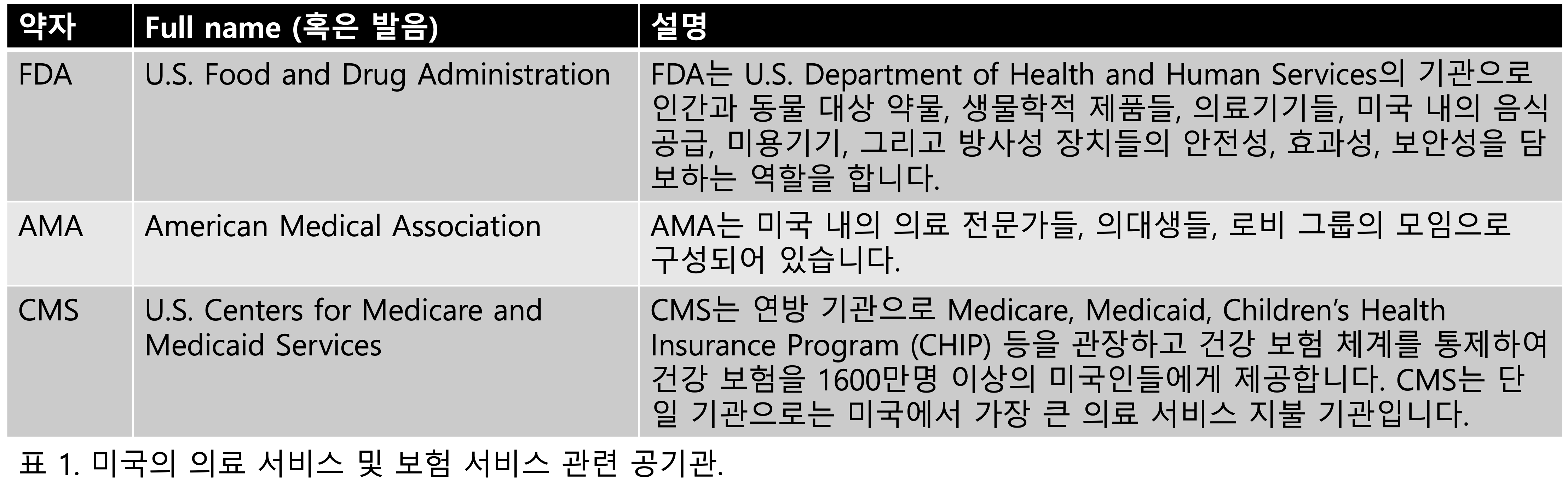
FDA는 미국 내에서 사용 및 처방되는 의료기기들의 안전성, 유효성을 검증하고 관할하는 역할을 합니다. 단, 여기서 주의할 점은 FDA의 인허가 통과는 의료기기가 안전하고 다른 동등 기기에 비해 열등하지 않다는 것을 증명하는 것일 뿐 실제로 의료기기가 의학적으로 의미있는 결과를 도출한다는 것은 아니라는 것입니다.
예를 들어, A라는 의료기기가 FDA 인허가를 받았다고 하면, 그 기기가 실제로 환자들을 더 살려주거나 예후를 좋게 만든다는 것은 아니라는 것입니다. 다만, A라는 의료기기는 단순히 환자에게 해를 끼치지 않는다는 것(no-harm principle)이 어느 정도 보장되었고 의사 혹은 기존의 의료기기에 비해 열등하지 않은 성능을 특정 그룹에서 보였다는 것을 말해줄 뿐입니다.
AMA는 미국 의사 협회로, 그 유명한 JAMA가 Journal of AMA라는 뜻입니다. AMA는 단순히 의학적 전문가들의 집단을 넘어 수가에도 영향을 미치게 되는데 의료 전문가들의 모임인 만큼 AMA에는 21명의 AMA 위원으로 구성되는 AMA CPT Editorial board라는 것이 있어(CPT는 아래에서 등장합니다.) 실제로 어떤 FDA를 통과한 의료기기가 의학적으로 의미있는 결과를 산출해내는지, 그래서 그 의료기기에 돈을 지불할 만한 가치가 있는지를 평가하는 역할도 수행하게 됩니다.
CMS는 Medicare과 Medicaid, CHIP으로 대표되는 미국 보험 지불의 주체입니다. Medicare는 미국 내 65세 이상 노령 인구에 보험을 제공하는 공보험이고, 말기 신장질환(end-stage renal disease; ESRD)과 같은 특정 질환을 가지는 젊은 층에도 보험을 함께 제공하고 있습니다. Medicaid는 aid(돕다)라는 단어가 시사하듯 미국 내 저소득층에 보험을 지원하는 사회보장 시스템입니다. CHIP은 말 그대로 청소년들에게 사회 보장 시스템을 제공하는 프로그램이고요. CMS는 위 표에 적힌 바와 같이 단일 기관으로는 미국에서 가장 큰 의료 서비스 지불 기관입니다. 미국 인구 중 8200만명이 Medicaid에 의해서 커버되고, 6900만명이 Medicare에 의해서 커버되며, 1200만명 정도는 Medicaid와 Medicare 둘 다에 의해서 커버됩니다(dually eligible).
그렇다면 미국에서 수가를 받는 것은 또 어떤 의미냐? 기본적으로 미국의 수가는 CPT라는 5자리 숫자+영어 알파벳 코드들의 집합입니다. CPT는 다시 Category I, II, III으로 나뉘는데, 이들은

로 구성되어 있습니다. CPT Cat I은 정식 수가 코드, Cat II는 보상 대상이 아닌 질관리 코드, Cat III은 혁신적인 기술들(영어로는 emerging techs)에 대한 임시 수가 코드입니다. 원칙적으로는 Category I만이 보상 대상이지만 실제로는 Category III도 꽤나 보상받는 경우들이 많은 것 같습니다. 이전에 제가 썼던 글을 보면 다음과 같은 table이 있는데,
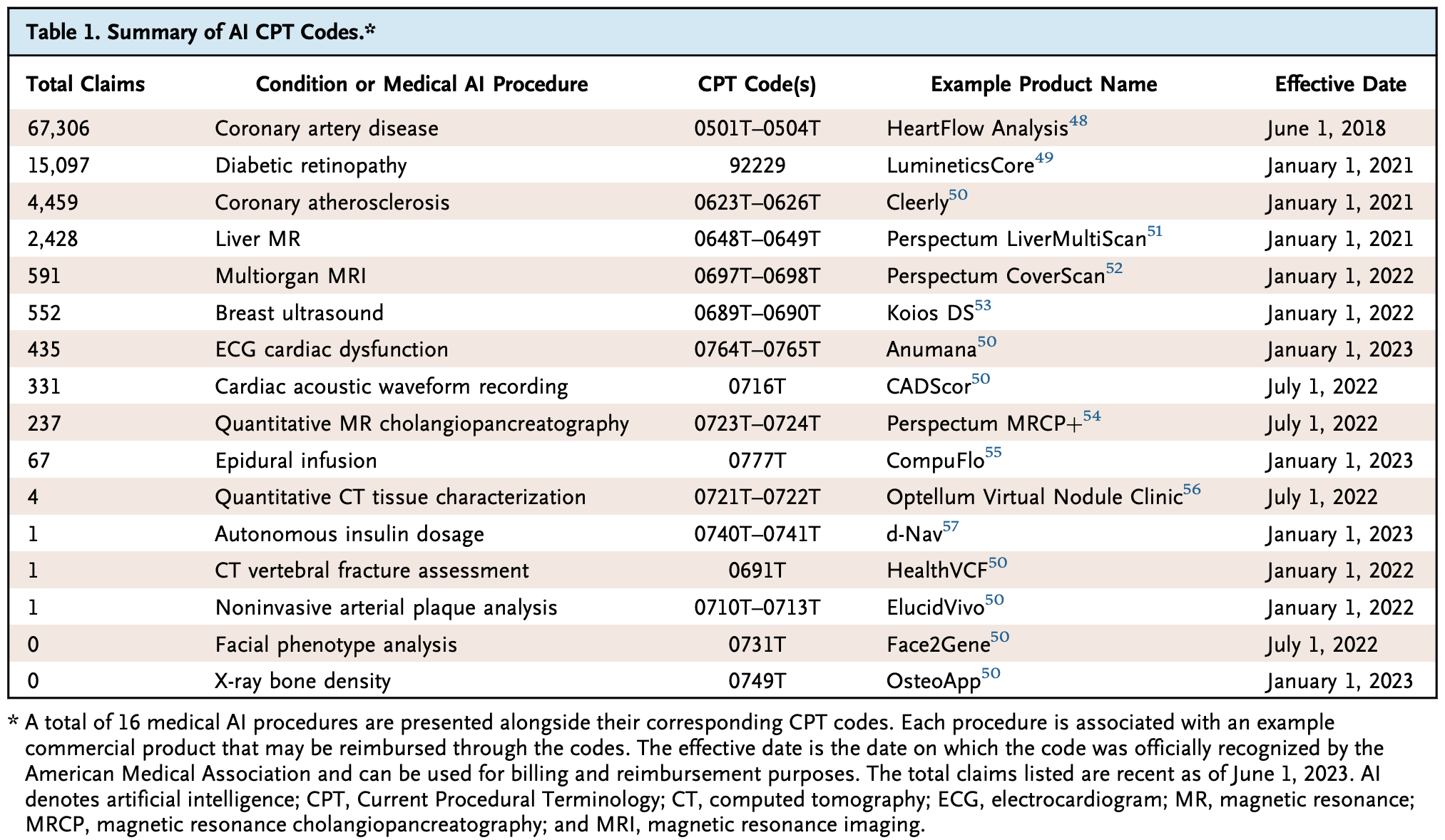
이들의 거의 대부분은 CPT Cateogry III으로, 5자리 코드의 맨 마지막에 T라는 글자가 적혀 있어서 temporary라는 것을 확인할 수 있습니다. 따라서 기본적으로는 보상의 대상이 아니지만, 사실상 AI SaMD (Software as a Medical Device)는 모두 보상되고 있는 중입니다.
이렇게 CPT 코드로 보상받기 위해서는 의료기기 인허가를 통과해야 합니다. 미국의 의료기기는 크게 세 가지 위험도로 분류되는데, 첫 번째가 저위험군인 Class I, 두 번째가 중등도 위험군인 Class II, 세 번째가 고위험군인 Class III입니다.
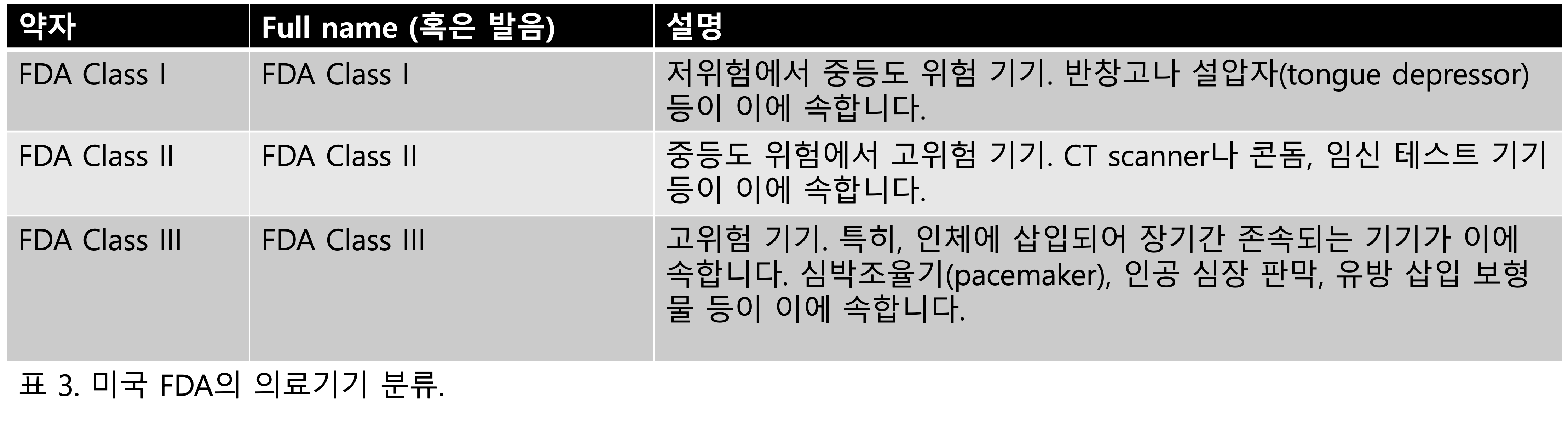
대부분의 AI SaMD는 Class I이나 II에 속하고 몇 가지 임상적으로 중요한 결정을 내리는 인공지능 의료기기들은 이론적으로 Class III에 속할 수 있습니다. 이렇게 의료기기의 등급을 나누는 이유는 관리의 목적도 있고 의료기기 인허가 트랙이 다르기 때문인데요, Class I, II는 510(k)나 De Novo 트랙을 타게 되지만 Class III의 경우에는 PMA를 타야 합니다.

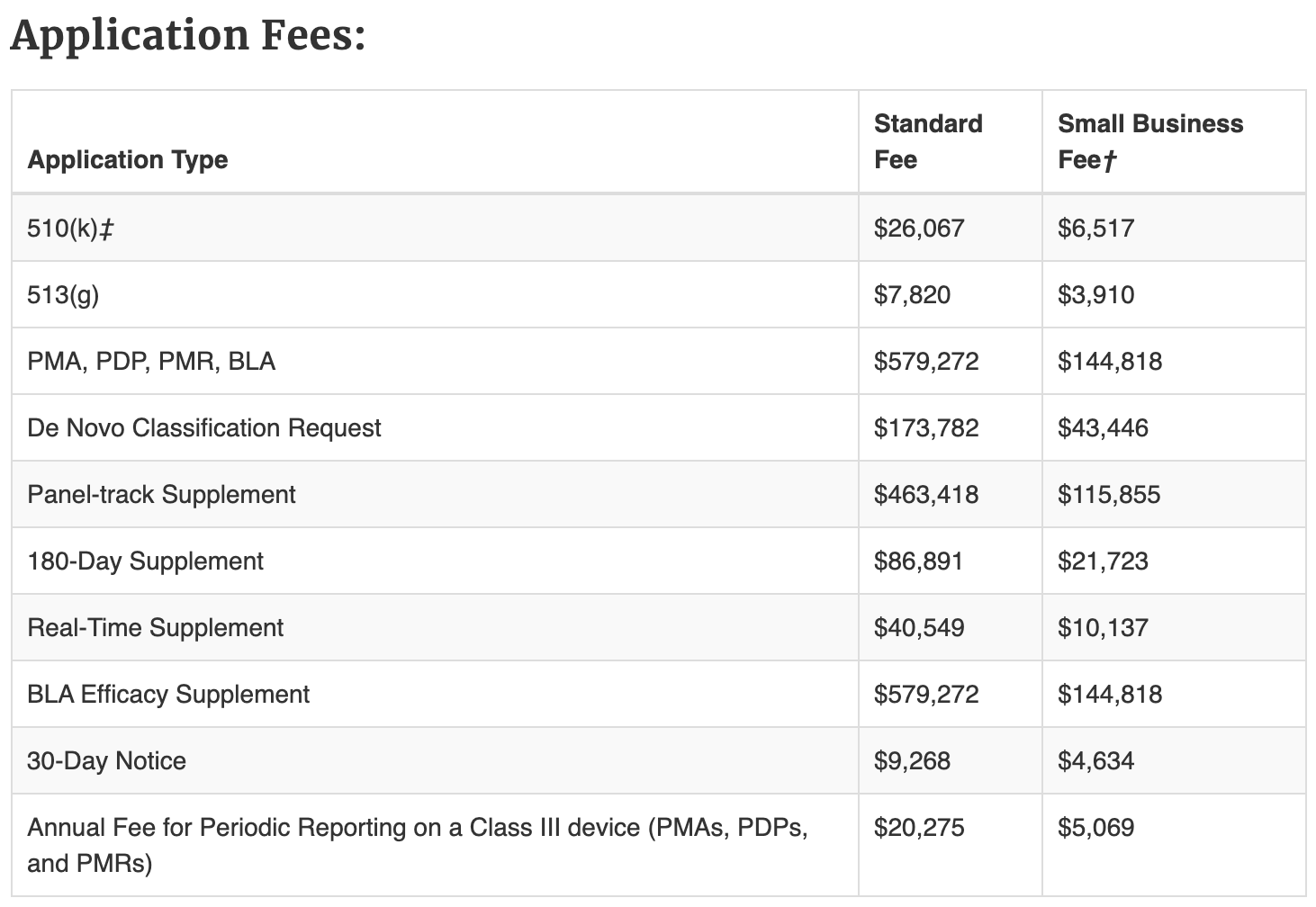
기존의 기기(=동등기기)가 있는 경우에는 510(k), 동등 기기가 없는 세계 최초의 기기는 De Novo, 그리고 FDA Class III에 해당하면 PMA를 타야 합니다. 사실 회사 입장에서 이들을 혁신성이나 동등 기기 존재 여부만으로 평가하기에는 부담이 있을수도 있는게, FDA 홈페이지를 참고하면 2025년 11월 29일 기준으로 FDA 510(k)는 중소기업 기준 6,517달러의 신청비가 들지만 De Novo는 43,446 달러로 거의 6~7배 정도 차이가 나게 되며 신청비가 만만치 않아 잘 고민하고 신청해야 합니다.
이렇게 미국 의료기기의 규제적 관점을 살펴보았습니다. 다음에 기회가 된다면 미국 내의 의료인공지능 수가 현황을 다뤄 보도록 하겠습니다.
